在天然细胞环境中,蛋白通过快速、可逆、精细的翻译后修饰调控其功能、亚细胞定位和稳定性。但基于抗体的传统分子识别工具由于穿膜效率、稳定性和免疫原性等的限制,难以用于在活细胞内原位捕获蛋白和解析其结构变化信息。为突破这一难题,赵美萍课题组利用分子印迹方法合成了一类高效的纳米捕手,实现了活细胞内目标蛋白的精准捕获,并揭示出其动态翻译后修饰的全新图景(图1)。该研究为活细胞内的蛋白研究提供了一种极具潜力、可替代抗体的全新纳米工具。
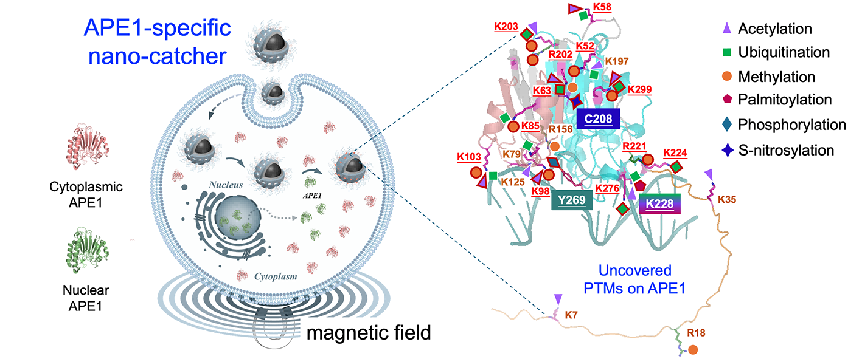
图1. 分子印迹纳米捕手在活细胞内精准捕获目标蛋白,揭示多功能蛋白APE1动态翻译后修饰的全新图景。
研究团队在早期工作中发现了一个有趣的现象:人类核酸修复蛋白脱碱基核酸内切酶1(APE1)与禽类蛋白亲和素(AVD)在进化上互不相干,但两者之间存在特殊的相互作用。基于这一发现,她们利用AVD作为分子伴侣构建的DNA荧光探针,成功实现了活细胞不同亚细胞区域中APE1的原位荧光成像(Nucleic Acids Res. 2017, 45, e45; 2024, 52, e41)。进一步,将APE1组装在AVD修饰的硅包磁纳米颗粒表面,通过聚多巴胺的分子印迹过程,获得了具有金属离子响应的APE1纳米抑制剂(J. Am. Chem. Soc. 2018, 140, 16925)。
为阐明APE1与AVD之间这种不寻常相互作用的结构基础,团队结合二维核磁共振、交联质谱、单分子荧光共振能量转移和荧光相关光谱等方法开展了系统研究(图2)。结果表明,APE1的“背面口袋”(Back Pocket)及DNA结合区域均参与了与AVD的相互作用。值得注意的是,这些区域与人类MUTYH(hMYH)蛋白在碱基切除修复通路(BER)中与APE1的已知相互作用界面高度相似。在AVD方面,其固有的生物素结合口袋区域参与了与APE1的作用;更关键的是,当生物素结合达到饱和后,口袋上方关键loop区的构象重排使AVD与APE1的结合更加紧凑和稳定。这一机制为后续构建APE1的定向分子印迹位点提供了结构稳定的界面基础。
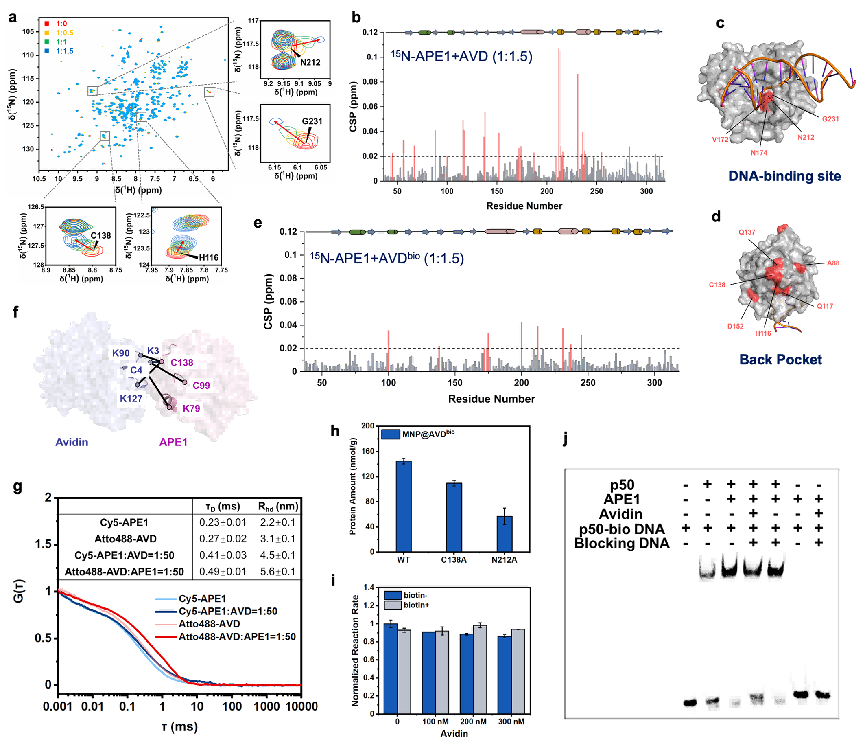
图2. 多模式分析表征APE1与AVD之间的相互作用。(a-e)NMR-TROSY谱图显示,APE1结合AVD后残基产生化学位移扰动,这些残基特异性地位于DNA结合区域和“背面口袋”区域;(f)交联质谱和(g)荧光相关光谱证实了蛋白复合物的形成;(h)突变分析鉴定出残基C138和N212对结合至关重要;(i-j)功能测定表明,AVD与APE1的相互作用可调节APE1的AP核酸内切酶活性,及其通过氧化还原作用对NF-κB p50亚基的激活。
研究团队通过对多巴胺聚合反应机理的深入研究发现,蛋白表面的局部构象会显著影响多巴胺及其氧化中间产物聚合过程,并找到了消除这一影响的途径。基于此,团队提出了“分层印迹‑精雕细琢”策略,用于合成更精准、抗干扰能力更强的APE1分子印迹识别材料(图3a)。她们首先采用柔性间隔臂将生物素共价接枝在硅包磁纳米颗粒表面,然后以生物素为锚点在纳米颗粒外围包覆单分子层的亲和素,并进一步结合生物素使其达到饱和。接下来加入APE1模板分子与生物素/亲和素提供的“软界面”结合,并引入羟基苯硼酸(B–OH)与APE1形成自组装体系,同时封闭AVD表面暴露于APE1结合界面之外的糖基。之后加入多巴胺进行表面印迹,形成对APE1的结构有“记忆效应”的印迹位点。聚合完成后,对外层非印迹区域进行致密亲水性封闭,然后利用含镁离子、DTT和非离子表面活性剂的洗脱缓冲液移除模板分子,即获得了能在复杂背景下快速识别和捕获APE1的磁性纳米颗粒(bMIPAPE1)。
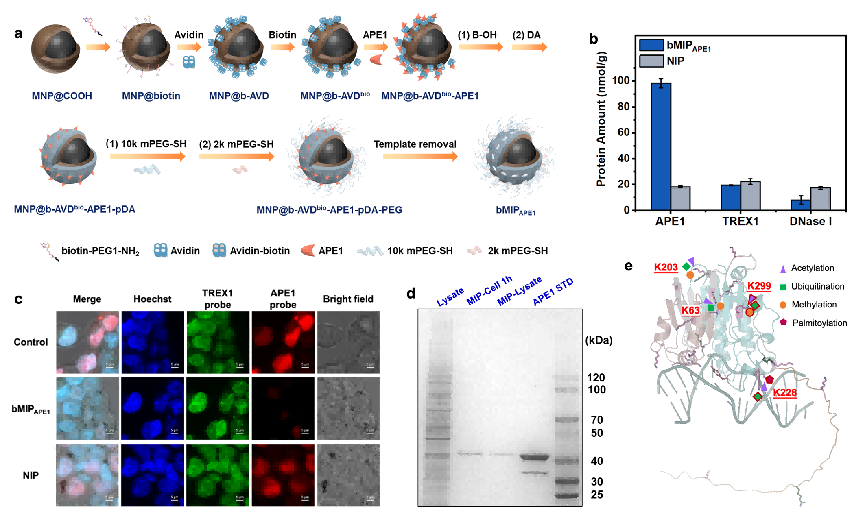
图3. bMIPAPE1的制备、性能表征及活细胞内APE1捕获与翻译后修饰解析。(a-c)bMIPAPE1的制备流程、对APE1的特异性识别能力、以及在活细胞内原位捕获APE1并抑制其功能活性的效果;(d)bMIPAPE1捕获产物的纯度鉴定。SDS-PAGE显示(泳道从左至右):细胞裂解液、活细胞内捕获回收的APE1、细胞裂解液中捕获回收的APE1、APE1标准品、蛋白Marker;(e)活细胞内APE1上多个翻译后修饰热点的鉴定结果,同一残基位点呈现出多样化的修饰景观。
体外结合实验表明,bMIPAPE1对 APE1表现出高选择性和高结合亲和力,而对结构相近的多种非靶标蛋白无明显非特异性吸附(图3b)。在磁场辅助下,bMIPAPE1不到30 分钟即可进入活细胞。荧光探针实验显示,bMIPAPE1捕获细胞质中的APE1后显著抑制其活性,继而诱导细胞核内的APE1向细胞质输出,从而使活细胞内APE1的整体水平下降(图3c)。bMIPAPE1从活细胞中捕获的APE1可在温和条件下重新释放,SDS-PAGE 分析显示其为高纯度的单一条带(图3d)。对不同培养条件下的捕获产物进行高分辨质谱分析,共鉴定到APE1上18个残基的25种尚未见报道的翻译后修饰(图1),其中多个位点同时存在多样化的修饰类型(图3e)。值得注意的是,APE1不仅是碱基切除修复(BER)通路的核心蛋白,还作为多种转录因子的氧化还原激活剂,并参与RNA加工等过程。该研究为深入理解APE1在活细胞内的功能调控机制打开了一扇全新的窗口。
相比于抗体方法,该纳米捕手能高效进入活细胞,对目标蛋白进行快速精准捕获,并有效地保护蛋白上低丰度、易丢失的动态翻译后修饰,为解析蛋白功能调控网络提供了全新工具。目前,研究团队正积极将该策略推广至更多目标蛋白,有望发展为一类普适性的活细胞蛋白捕获与功能调控研究平台,为揭示疾病发生机理和发现新药物靶点提供有力支撑。
上述研究成果于2026年4月8日在线发表于《核酸研究》(Nucleic Acids Research)期刊,题为“Live-cell decoding of labile post-translational modifications in APE1 with a rationally engineered nano-catcher”。与该研究相关的发明专利已于2026年3月20日正式获得授权。北京大学化学与分子工程学院赵美萍教授为该论文的通讯作者,已毕业博士张芮兰、解怀萱和在读博士生祝晨旭为该论文的共同第一作者。北京核磁中心的金长文教授、李红卫老师和牛晓刚老师指导并合作完成了其中的核磁共振波谱分析工作。北京大学分析测试中心(PKUAIC)的关妍老师、周文老师和刘莹老师在荧光成像和质谱分析中提供了重要帮助。该研究得到国家自然科学基金、国家重点研发项目和北京分子科学国家研究中心的资助与支持。
原文链接:
https://academic.oup.com/nar/article/54/6/gkag323/8644115
排版:高杨
审核:牛林,刘志博